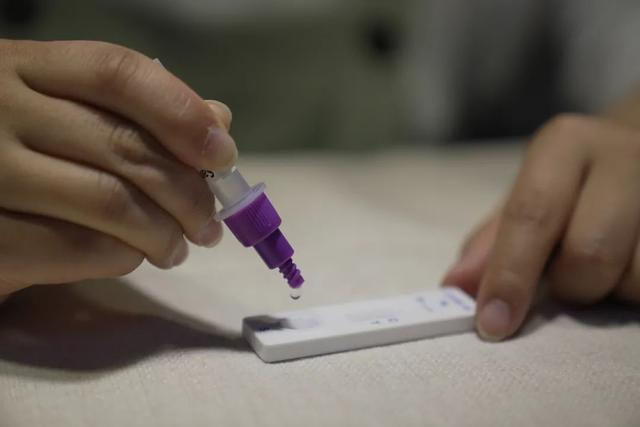
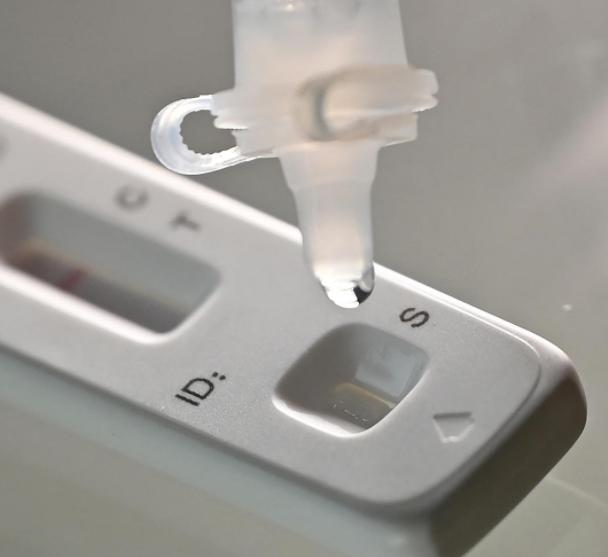
El 12 de marçth 2022, elNMPA (SFDA) va emetre un avís aprovant el canvi de sol·licitud per a l'autoprova de productes d'antigen COVID-19 per part de Nanjing Vazyme BiotechCo, Ltd, Tecnologia de bioenginyeria Jinwofu de BeijingCo, Ltd, Shenzhen Huada Yinyuan Pharmaceutical Technology Co., Ltd, Guangzhou Wondfo Biotech Co., Ltd iBeijing Savant Biotechnology Co, Ltd(Huaketai).S'han llançat cinc productes d'autoprova d'antigen COVID-19.
L'11 de març de 2022, l'NHC havia anunciat que, per tal d'optimitzar encara més l'estratègia de prova del nou coronavirus i atendre les necessitats de prevenció i control de la COVID-19, l'equip integral del mecanisme conjunt de prevenció i control del Consell d'Estat va decidir afegir prova d'antígens a proves d'àcids nucleics i va fer "el protocol d'aplicació per a la detecció d'antígens de nou coronavirus (assaig)"
El protocol especifica la població aplicable per a la prova d'antígens:
En primer lloc, aquells que visiten institucions mèdiques primàries i presenten símptomes com vies respiratòries i febre dins dels 5 dies posteriors a l'aparició dels símptomes;
En segon lloc, el personal d'observació de la quarantena, inclosa l'observació de la quarantena a casa, el contacte proper i el contacte subestret, l'observació de la quarantena d'entrada, l'àrea de contenció i el personal de l'àrea de control;
El tercer són els residents de la comunitat que tenen la necessitat d'autodetecció d'antigen.
Consells: la detecció d'antígens és un complement important de la detecció d'àcids nucleics, però els resultats de l'autodetecció d'antigens no es poden utilitzar com a base per al diagnòstic de la infecció.
Hora de publicació: 22-mar-2022